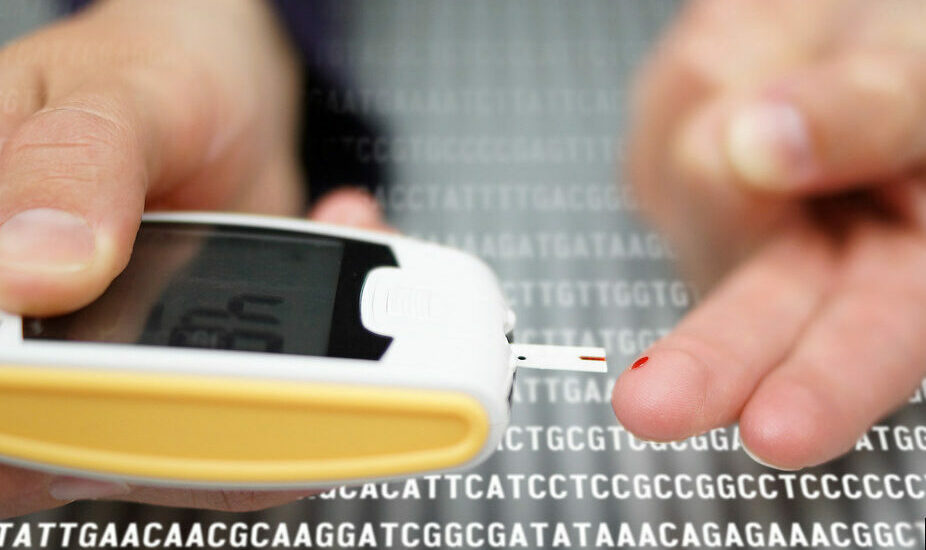
La statunitense Food and Drug Administration (Fda) ha approvato il Tzield (teplizumab-mzwv), il primo farmaco, co-prodotto da Provention Bio e Sanofi, in grado di rallentare l’esordio del diabete di tipo 1 di stadio 3 negli adulti e nei bambini a rischio.
Il diabete 1 è una forma autoimmune in cui il sistema immunitario danneggia la porzione di pancreas responsabile della produzione di insulina.
CHI POTRÀ RICEVERLO
La Fda ha autorizzato l’utilizzo di questa nuova terapia dagli 8 anni in su per quei pazienti che sono affetti dal diabete di tipo 1 di stadio 2, al fine di rallentare l’insorgenza dello stadio 3.
Il via libera al Tzield “aggiunge una nuova importante opzione terapeutica per alcuni pazienti a rischio”, ha dichiarato John Sharretts, direttore della Divisione di Diabete, Disturbi Lipidici e Obesità del Centro per la Valutazione e la Ricerca sui Farmaci della Fda. “Il potenziale del farmaco di ritardare la diagnosi clinica del diabete di tipo 1 può offrire ai pazienti mesi o anni senza gli oneri della malattia”.
Negli studi clinici, scrive la Cnn, Tzield ha ritardato la progressione di poco più di due anni, ma i benefici sono durati molto più a lungo in alcuni dei partecipanti allo studio.
LO STUDIO
La sicurezza e l’efficacia di Tzield, riferisce la Fda, sono state valutate in uno studio randomizzato, in doppio cieco, condotto su 76 pazienti con diabete di tipo 1 di stadio 2.
Durante il trial, alcuni pazienti hanno ricevuto il farmaco e altri un placebo una volta al giorno per infusione endovenosa per 14 giorni.
I RISULTATI
Nel follow-up è risultato che il 45% dei 44 pazienti che avevano ricevuto il Tzield avevano sviluppato diabete di tipo 1 di stadio 3 più tardi rispetto al 72% dei 32 pazienti che avevano ricevuto un placebo.
Il tempo medio dalla randomizzazione alla diagnosi è stato di 50 mesi per i pazienti che hanno ricevuto Tzield e di 25 mesi per quelli che hanno ricevuto un placebo. “Questo – conclude la Fda – rappresenta un ritardo statisticamente significativo nello sviluppo del diabete di tipo 1 allo stadio 3”.
COME FUNZIONA
Tzield, si legge nella nota della Fda, si lega ad alcune cellule del sistema immunitario e ritarda la progressione verso il diabete di tipo 1 di stadio 3. È in grado di disattivare le cellule immunitarie che attaccano le cellule produttrici di insulina, aumentando al contempo la percentuale di cellule che aiutano a moderare la risposta immunitaria.
Il farmaco, come nel trial, viene somministrato per infusione endovenosa una volta al giorno per 14 giorni consecutivi.
CHI LO PRODUCE
Tzield viene prodotto dalla statunitense Provention Bio, che a ottobre ha annunciato un accordo di co-promozione con Sanofi per il lancio negli Stati Uniti.
QUANTO COSTERÀ
Stando alla Cnn, che ha riportato un colloquio tra il produttore e gli investitori, il costo di produzione di un ciclo completo di trattamento sarà di circa 194.000 dollari, ma si prevede che questo non sarà il prezzo che pagheranno i consumatori.
IL DIABETE DI TIPO 1
Il diabete di tipo 1, spiega la Fda, è una malattia che si manifesta quando il sistema immunitario attacca e distrugge le cellule che producono l’insulina. Le persone affette da questa malattia hanno un aumento del glucosio che richiede iniezioni di insulina (o l’uso di un microinfusore di insulina) per sopravvivere e devono controllare regolarmente i livelli di zucchero nel sangue durante la giornata.
Sebbene possa comparire a qualsiasi età, il diabete di tipo 1 viene solitamente diagnosticato nei bambini e nei giovani adulti. Una persona è più a rischio se ha un genitore, un fratello o una sorella che ne soffrono, ma la maggior parte dei pazienti in genere non presenta familiari con diabete di tipo 1.
Nel 2019, negli Stati uniti, secondo l’American Diabetes Association, circa 1,9 milioni di persone avevano il diabete di tipo 1, tra cui 244.000 bambini e adolescenti.
PERCHÉ È IMPORTANTE RALLENTARE LA MALATTIA
“L’insorgenza del diabete di tipo 1 di stadio 3 è un momento che cambia la vita: una volta che le cellule produttrici di insulina non sono più in grado di mantenere un normale controllo glicemico, questa condizione irreversibile può portare il paziente a dover fare, in un solo anno, 1.460 punture al dito per controllare i livelli di glucosio nel sangue, circa 1.100 iniezioni di insulina e a sperimentare una media di 127 episodi di ipoglicemia”, ha spiegato Eleanor Ramos, responsabile medico di Provention Bio.